La corsa verso il farmaco
{loadposition addthis}
La ricerca verso una cura per la SMA muove passi importanti grazie all’impegno dei ricercatori e delle casa farmaceutiche, al momento sono in corso trial sull’uomo, su bambini affetti e su volontari sani, per i test di sicurezza. Ci sono diverse strategie tutte con lo stesso obiettivo, aumentare la produzione di proteina SMN efficiente, attraverso farmaci a piccole molecole (small molecule drugs), terapie antisenso e vettori virali che agiscono su target diversi. L’obiettivo che, ovviamente, i ricercatori si pongono è la cura, specialmente per i bambini SMA 1 ma, ciò che realisticamente si può fare in breve tempo, sarà un rallentamento o lo stop della progressione della malattia. Grazie a questi vari approcci terapeutici l’ottimismo aumenta sempre più nei ricercatori.
Il farmaco della ISIS, soprannominato SMNRx, lavora per incrementare i livelli di proteina SMN agendo sullo splicing dell’esone 7 su SMN2. Nella SMA, a causa di una mutazione del gene SMN1, si ha una carente o assente produzione di proteina SMN, responsabile della sopravvivenza dei motoneuroni. Nel genoma umano è presente un gene quasi identico, chiamato SMN2, che differisce dal SMN1 per un singolo nucleotide nell’esone 7. Questa piccola differenza porta ad una grande conseguenza: a causa dello “splicing” dell’esone 7 durante la trascrizione si ha la produzione una proteina SMN più corta e meno stabile che degrada velocemente. Nella fase I del trial ISIS, iniziata nel dicembre 2011, è stata somministrata una singola iniezione di SMNRx alla base del midollo spinale in 28 bambini con SMA di tipo 2 e 3. La terapia consiste in una sequenza di DNA di 18 nucleotidi che corregge l’anomalo splicing, “spostiamo alcune proteine regolatorie negative che consentono il meccanismo di splicing” spiega Frank Bennet, il capo ricerca all’ISIS. SMNRx su modelli animali migliora la forza muscolare nei test comportamentali e aumenta la vita media. “Pensiamo di avere un farmaco che avrà un grande impatto sulla malattia” ha detto sempre Bennet. Claudia Chiriboga della Columbia University afferma “Sono molto ottimista, per una volta abbiamo trovato un timing ed un dosaggio ottimale, stiamo per vedere risultati che cambieranno la vita”. Altre ditte, quali Novartis, Roche e Paratek, stanno sviluppando dei farmaci a piccole molecole designati ad aumentare l’inclusione dell’esone 7 nel trascritto di SMN2.
Prima di adottare la strategia della correzione dello splicing, altri ricercatori hanno provato ad aumentare i livelli di proteina SMN in diversi modi. Tra questi abbiamo l’utilizzo degli inibitori istone deacitilasi (bloccanti-HDAC) che, come è stato dimostrato su modelli animali, potrebbero promuovere l’espressione genica di SMN2. Però, anche se sono stati riportati dei casi di bambini con grandi miglioramenti, in due trial clinici con acido valproico vs placebo non si è riscontrato un vantaggio clinico.
Il NINDS di Bethesda ha identificato un composto, soprannominato ALB-111, che crea una proteina SMN estesa che, anche se mancante dell’esone 7, potrebbe avere funzionalità o aiutare a stabilizzare le proteine complete. Si sta cercando di vedere se questo farmaco possa avere un’approvazione per un ulteriore sviluppo.
Repligen ha sviluppato un farmaco chiamato RG3039 che, bloccando l’enzima DcpS, porta ad un aumento di livelli di SMN trascritto, sia troncato che completo. Anche RG3039 ha mostrato risultati promettenti in studi su modelli animali. Si è da poco conclusa la fase I,a di un trial clinico con somministrazione di una singola dose di RG3039 in 32 volontari sani e i risultati hanno portato ad affermare che la preparazione liquida è sicura e che inibisce DcpS nelle cellule del sangue. Una fase 1b per testare la sicurezza della dose multipla è iniziata a settembre, sempre su 32 volontari sani.
Una strada alternativa è quella della terapia genica con la somministrazione di virus modificati che trasportino copie funzionanti del gene SMN1. Utilizzando un virus adeno-associato come vettore sono state introdotte con successo copie extra della sequenza che codifica per la proteina SMN umana in modelli di topo con SMA. Non solo questo ha portato ad un aumento della durata della vita degli animali, ma ha anche ripristinato la funzione motoria quasi a livelli normali. Il composto virale è stato iniettato anche su maiali e scimmie con pochi effetti collaterali. I ricercatori stanno preparando un dossier tossicologico e farmacocinetico necessario per procedere con la sperimentazione.
E’ importante capire la giusta via di somministrazione, i tessuti che devono essere raggiunti dalla terapia e il timing. Sembra infatti che per avere un miglior effetto della terapia e della prospettiva di vita su modelli animali sia necessario raggiungere alti livelli di SMN anche nei tessuti periferici ed una somministrazione precoce.
Sembra essere emerso che la SMA potrebbe non riguardare solo i motoneuroni, ma anche i muscoli periferici ed altri tessuti. Se questa ipotesi venisse confermata vorrebbe dire che i farmaci dovrebbero agire su tutto l’organismo, non solo nel sistema nervoso centrale, per avere il massimo effetto terapeutico. “Se vanno nel cervello, vanno in ogni altra cellula del corpo” dice Luca Santarelli della Roche riguardo i farmaci a piccola molecola, è più complicato invece per l’approccio Isis in quanto la somministrazione avviene direttamente nel sistema nervoso centrale. Sebbene sia stato osservato che la somministrazione di Isis nel cervello ha quasi raddoppiato la durata della vita nei modelli animali, la somministrazione sistemica invece ha aumentato la sopravvivenza da 2 settimane a 8 mesi. Questo risultato porta a dire inequivocabilmente che necessitiamo di alti livelli di SMN in tutto l’organismo.
Oltre al luogo di somministrazione c’è anche il problema del timing. E’ stato dimostrato, sempre in studi su modelli animali, che prima avviene la somministrazione del farmaco, migliore è l’effetto e più lunga la prospettiva di vita.
Isis è stato somministrato solo a bambini con più di 2 anni, ma ci si aspetta di somministrarlo già nei primi mesi di vita o prima dello sviluppo dei sintomi.
Ora c’è più speranza per un trattamento della SMA in un futuro vicino, più che in qualsiasi altro momento” (Karen Chen, SMA Fundation)
Fonte: Elie Dolgin, Nature Medicine, Call in backup 2012, volume 18, n 11, pp. 1602-1605. Liberamente tradotto da F. Braguti e A. Pallara
16th Annual International Spinal Muscular Atrophy – Family of SMA (Dott. Danilo Tiziano – 8 settembre 2012 VIII Convegno annuale Famiglie SMA APS ETS – ASAMSI)
Ormai sono cinque i potenziali farmaci contro la SMA entrati nello sviluppo clinico. La pipeline del farmaco SMA continua ad aggiornarsi: eccone l’ultima versione!
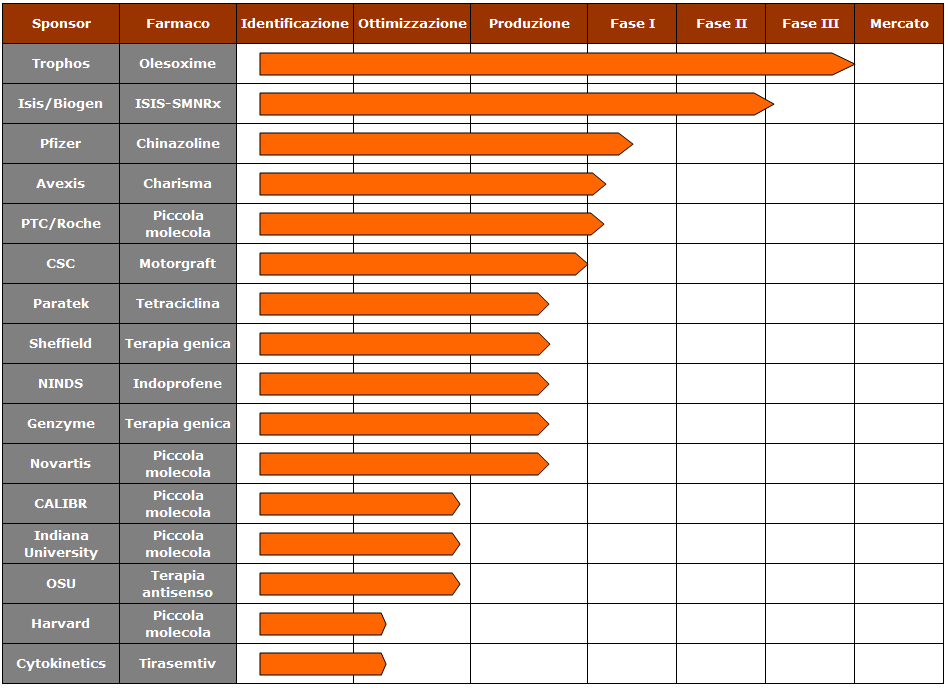
Se vuoi sapere di più visita il nostro sito della Ricercasma e il sito di Families of Sma.
NOTIZIE IN EVIDENZA
Segreteria Famiglie SMA: chiusura di fine anno
La violenza contro le donne con disabilità: una realtà invisibile
Quota Associativa Soci Famiglie SMA 2025
lunedì 9 dicembre 2024 | Webinar | Incontro online con le SMAestre e SMAprof
da Famiglie SMA è arrivato il Natale
Incontro online per i genitori di Famiglie SMA
Malattie genetiche rare: esperti, pazienti e Istituzioni a confronto sulle necessità più urgenti
Due nuove poltrone letto al Policlinico di Bari
Online il nuovo vademecum scuola
Segreteria Famiglie SMA: chiusura di fine anno
La violenza contro le donne con disabilità: una realtà invisibile
Quota Associativa Soci Famiglie SMA 2025
lunedì 9 dicembre 2024 | Webinar | Incontro online con le SMAestre e SMAprof